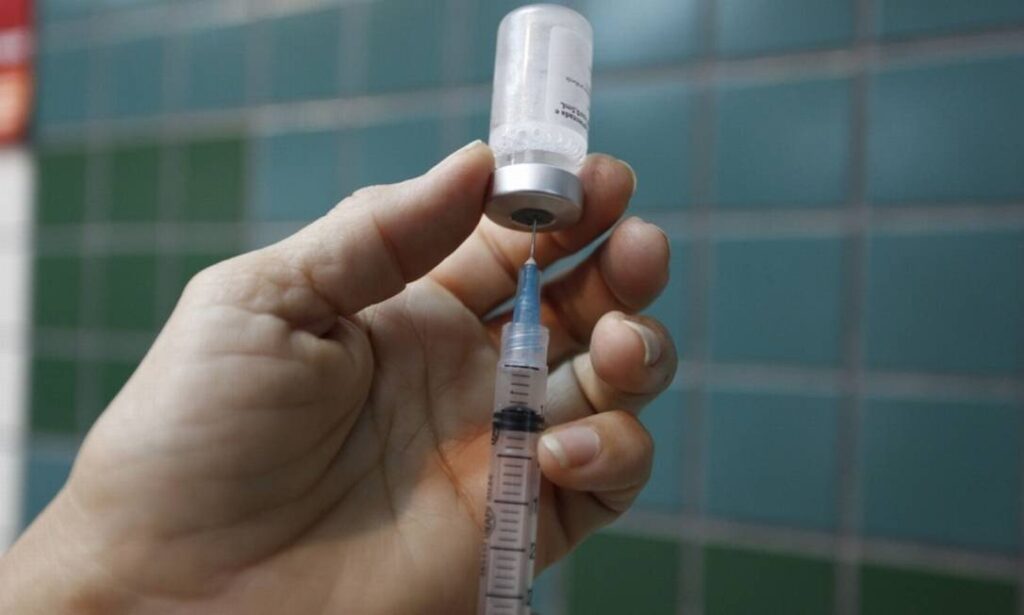
A empresa farmacêutica multinacional, Pfizer e a BioNTech receberam autorização da Agência Nacional de Vigilância Sanitária (Anvisa) nessa terça-feira (21), para fazer testes da vacina contra o novo coronavírus (Covid-19) no Brasil. A autorização foi publicada no Diário Oficial (DO).
A Anvisa afirmou que 29 mil pessoas farão parte do estudo clínico fase III da vacina, sendo que desse total, 5 mil estão no Brasil. O estudo será feito em São Paulo e na Bahia, ao passo que a seleção dos voluntários será responsabilidade das companhias.
“O ensaio clínico aprovado é um estudo controlado com placebo, randomizado, cego para o observador, de determinação de dose, para avaliar a segurança, a tolerabilidade, a imunogenicidade e a eficácia da vacina”, destacou o comunicado da Agência.
De acordo com uma prévia de um artigo publicado ontem no ‘medRxiv’ , a vacina de coronavírus que está sendo desenvolvida pela BioNTech junto com a Pfizer se mostrou promissora na primeira fase. Contudo, o artigo é uma pré-impressão e ainda não foi certificado pela revisão, o que é necessário para ser publicado formalmente em revistas científicas.
Vacina de Coronavírus pode ser aprovada neste ano, diz regulador da UE
O responsável por anti-infecciosos e vacinas da Agência Europeia de Medicamentos (EMA, em inglês), Marcos Cavaleri, afirmou nesta terça-feira que os órgãos reguladores europeus podem aprovar a primeira vacina contra o coronavírus ainda neste ano. Isso pode acontecer por conta dos resultados promissores de diversos testes que foram feitos por farmacêuticas recentemente. As informações são da agência “Bloomberg”.
“Estamos nos preparando para essa possibilidade, para que nós, como reguladores, estejamos prontos. Será uma questão de ver se esses dados podem ser suficientes para permitir qualquer tipo de aprovação até o final de 2020”, afirmou Cavaleri em entrevista publicada pela agência.
Veja também: Coronavírus: universidade russa conclui com sucesso teste de vacina
A EMA pretende avaliar os dados dos ensaios, as decisões clínicas e de fabricação em tempo real para tornar o processo de aprovação da vacina ainda mais rápido.
Notícias Relacionadas